发布日期:2018-11-07 11:52 来源:活性炭网 作者:活性炭网 浏览数:
抽象 通过超临界萃取啤酒花后残留物理活化得到的介孔活性炭HPA表面的聚(丙烯酸)(PAA)吸附层的纳米结构进行了表征。 该表征基于对固体颗粒的吸附聚合物量,表面电荷密度和z
在固 - 液界面上形成的聚合物吸附层的具体结构决定了胶体悬浮液的表面性质。这是在人类活动(即,环境,农业和工业应用)的许多领域普遍发生的高度分散的系统的稳定性十分重要的[ 1 - 8]。在固体表面上获得所需的聚合物层结构的可能性是由于大分子可以呈现大量不同的构象。聚合链的独特构象是原子或原子团围绕单键旋转的结果。它定义了聚合物在溶液中的行为,并且是由大分子与溶剂分子的相互作用产生的。
聚合物链(特别是分类为离子聚合物的那些)的构象可受许多因素的影响,其中最重要的因素如下:溶液的pH和离子强度; 温度; 聚合物的类型,分子量,浓度和多分散性; 和固体的类型,纯度和表面性质。改变和控制一个或多个参数,可以获得固体悬浮液,其特征在于对于特定的实际应用所需的稳定性。
非离子(即聚(乙二醇),聚乙烯吡咯烷酮,聚(丙烯酸) - 官能团在水溶液中不会发生解离)和离子(即聚(丙烯酸),聚丙烯酰胺,聚氨基酸,蛋白质 - 其大分子含有离子化基团)的聚合物在基础研究中使用含有无机氧化物[系统9 - 13 ]。它们如下:氧化硅(IV),氧化锆(IV),氧化钛(IV),氧化锰(IV),氧化铝(III),氧化铬(III)和氧化铁(III)。天然和合成沸石也广泛地研究[ 14 - 16]。这种系统有各种各样的可能的应用,在化妆品,药物,涂料的生产,医药如植入物和药物载体的部件,以及水处理技术和矿物加工[ 16 - 21 ]。
活性炭是一类吸附剂,对许多实际应用很重要。它们具有通常高度发达的表面积,其值可高达1500m 2 / g。毛孔的形状和大小是多种多样的。它们可以是两侧的开放通道,墨盒形,V形和具有平行或不平行壁的槽的形式。考虑到孔的大小,将它们分成三种类型:微孔(低于2nm),中孔(2-50nm)和大孔(高于50nm)碳。最常用的制备活性炭的原料是煤[ 22]。用于大规模生产的其他原料如下:椰子壳和木材。目前,诸如水果石或坚果壳之类的废物正变得越来越重要[ 23 ]。
活性炭广泛用于通过吸附SO 2,SO 3,H 2 S,CS 2,NH 3,NO x和其他有毒化合物来去除工业废气。从脂族和芳族烃类,酚类和它们的衍生物,农药,清洁剂,重金属,细菌,病毒,染料和低分子量有机化合物的废水净化也是活性炭应用[的一个重要领域24,25 ]。
关于聚合物质吸附的活性炭的使用在科学文献中极少报道。因此,本文的目的是测定在低分子量聚(丙烯酸)物理活化过程中超临界萃取啤酒花后从残留物中获得的活性炭(HPA)的吸附性能。
由于聚(丙烯酸)在水中具有优异的溶解性,无毒,并且与人体肌肉组织具有生物相容性,因此在食品加工,医药和许多工业部门(化妆品,药品,油漆,颜料,和纸张生产)[ 1,3 ]。PAA与各种聚合物(即聚(乙烯醇),聚乙烯吡咯烷酮,壳聚糖,纤维素)形成pH敏感和温度敏感的水凝胶。他们发现主要使用在控制药物释放系统[ 26,27 ]。PAA应用的其他方向包括废水净化,矿物加工,金属离子回收以及农业土壤质量的改善[5,7,8]。
施加的活性炭是由植物废料制备的低成本吸附剂,因此,它与其他更昂贵的吸附剂相比具有竞争力。另外,关于确定活性炭表面上的聚合物吸附层的纳米结构的研究可以在其未来应用中有助于就大分子化合物结合而言。
原料是超临界萃取尺寸为0.10-0.75mm的啤酒花(H)粉末后的残留物,空气干燥状态下的水分含量为5.6%。首先将初始材料在500℃下进行热解(P)过程。它在通过水平炉在氮气流下加热的石英管式反应器中进行,流速为170mL / min。在最终温度下,将样品保持1小时,然后在惰性气氛中冷却。然后,将炭在800℃的温度下在二氧化碳流(速率流250cm 3 / min)下进行物理活化(A)1小时。吸附剂表示为HPA。
为了除去沉积在吸附剂表面上的矿物质,用双蒸水洗涤活性炭以获得约2μS/ cm的上清液电导率(电导率计CDM 83,Radiometer)。
通过使用氮吸附/解吸方法(Accelerated Surface Area and Porosimetry ASAP 2405 Analyzer,Micrometritics Inc.,USA)测定固体BET表面积,孔体积和平均孔径。
使用高分辨率扫描电子显微镜Quanta 3D FEG(FEI,Field Electron and Ion Co.)获得活性炭的SEM图像。
CSDA样品的热分析在Simultaneous Thermal Analyzer STA 449 Jupiter F1(Netzsch,Germany)上在以下操作条件下进行:加热速率10℃/ min,氮气流速50cm 3 / min,温度范围温度为30-950°C,样品重量约为18 mg,传感器热电偶类型为S TG-DSC。在材料分解过程中排出的气态产物通过FTIR光谱仪(Brucker,德国)和四线质谱仪QMS 403C(Aeölos,德国)在线耦合到STA仪器进行分析。QMS数据收集在10至300amu的范围内。FTIR光谱记录在600-4000cm -1的光谱范围内,每个光谱16次扫描,分辨率为4cm -1。
根据Boehm方法评估酸碱表面性质[ 28 ]。使用体积(0.1mol / dm 3)标准HCl和NaOH(Avantor Performance Materials Poland SA)作为滴定剂。
活性炭的物理化学特性见表 1。另外,活性炭颗粒的SEM图像如图1所示 。
HPA活性炭的理化特性
| 参数 | 值 |
|---|---|
| BET比表面积[m 2 / g] | 1169 |
| 总孔容[cm 3 / g] | 0.66 |
| 微孔体积[cm 3 / g] | 0.29 |
| 平均孔径[nm] | 2.26 |
| pH值 | 5.5 |
| 酸性基团含量[mmol / g] | 0.47 |
| 基本组含量[mmol / g] | 1.57 |

活性炭的SEM图像
聚(丙烯酸)-PAA(Fluka),具有两个平均分子量的重量
对于p ķ的值确定,PAA溶液(100ppm的)在支持电解质(氯化钠,0.01摩尔/分米3)中的溶液用NaOH溶液(0.1摩尔/分米滴定3)。获得的滴定曲线表示溶液pH与加入的碱的体积(V b)的相关性,使得能够指定对应于滴定终点(V ep)的NaOH体积。将p K a值确定为pH值,其中V b = 1 / 2V ep。
PAA官能团在pH 3下的解离是最小的(解离度(α)等于0.03),而在pH 4.5,离子化和中性羧基的数量是相同的(解离度达到值0.5)。聚合物链的总电离发生在pH6和9(分别为α = 0.97和α = 0.99)[ 26 ]。
在25℃下在NaCl溶液中(浓度为0.01mol / dm 3)在三个溶液pH值(3,6和9±0.1)下进行吸附测量。首先,制备浓度范围为20-500ppm的聚(丙烯酸)溶液的六个系列(每种聚合物分子量不同的PAA样品三个)。然后,将0.1g活性炭引入每种聚合物溶液中。使用pH计(Beckman Instruments)调节所检查的悬浮液的适当pH值。吸附过程在连续振荡24小时的条件下进行。接下来,使用微量离心机(MPW Med.Instruments)离心固体,收集上清液用于进一步分析。
从吸附过程之前和之后溶液中聚合物浓度之间的差异(使用校准曲线)获得吸附的PAA的量。使用由Crummet和Hummel [ 30 ] 提出的聚(丙烯酸)与hyamine的反应。使用UV-VIS分光光度计Cary 100(Varian),在从与hyamine的PAA反应开始15分钟后,在波长500nm下测量所获得的浊度。
电位滴定使得能够确定固体表面电荷密度作为溶液pH的函数。为了获得支持电解质曲线(作为pH变化与添加碱的体积的关系),将50cm 3氯化钠溶液(0.01mol / dm 3)置于恒温容器中并用NaOH溶液(0.1滴定)滴定。 mol / dm 3)[ 31 ]。然后,使用0.035g活性炭以类似方式获得悬浮曲线。接下来,在HPA-NaCl-PAA系统中以100和500ppm的聚合物浓度进行电位滴定。
通过使用由恒温特氟龙容器,玻璃和甘汞电极(Beckman Instruments),pH计PHM 240(辐射计),实验室搅拌器,恒温器RE 204(Lauda)组成的组在25℃下测定固体表面电荷密度。 ,自动微量滴管Dosimat 765(Metrohm),以及由W.Janusz教授撰写的特殊软件“titr_v3”的计算机。
通过将0.01g固体加入到100cm 3的支持电解质或聚合物溶液(浓度为100或500ppm)中来制备用于ζ电位测量的活性炭悬浮液(不含和含有PAA )。使用超声波发生器XL 2020(Misonix)将悬浮液超声处理5分钟。然后,将溶液分成七份并倒入Erlenmayer烧瓶中,然后调节适当的pH(3,4,5,6,7,8,9±0.1)。使用Zetasizer Nano ZS(Malvern Instruments)在25℃下测量以这种方式制备的系统的ζ电位。使用Smoluchowski方程[ 32 ] ,基于液体介质中固体颗粒的电泳迁移率计算Zeta电位值。
对于电泳迁移率测定,使用激光多普勒电泳技术。带电粒子在电场中的运动基于多普勒效应来表征。确定从移动的粒子散射的光的频移。为此目的,从单个光源发射的激光束被分成两个相互相干的光束。其中一个通过粒子散射(散射光束),而后一个(参考光束)绕过测量单元。这两个光束叠加,发生干涉。它产生的调制信号的频率等于参考光束和散射光束的频率之差。差异很大,相当于高电泳迁移率。
图 2显示了活性炭热分解的TG,DSC和DTG曲线。在氮气氛中的HPA加热过程中可以区分四个阶段。第一个 - 在30-180°C范围内,最小值为103.1°C,重量损失为1.53% - 是吸热的。它主要与物理吸附水的去除和碳羧基的初始分解有关[ 33 ]。第二阶段的温度范围为180-550°C,DTG曲线上的最低温度为251.3°C,重量损失为2.3%。这种现象与表面基团的分解有关,例如羧基和含硫的表面基团(例如,硫 - 氧,硫化物,苯通过二硫桥与表面结合)[ 34]]。在550-850℃的温度范围内(最低751.1℃,重量损失为6.9%),表面基团(内酯,醌和羧酸酐)发生进一步的碎片整理。最后的温度范围,即850-945℃,与1.48%的重量损失相关。除了前一阶段的工艺特征之外,在高于800℃的温度下,可能发生强结合表面基团(例如羰基,吡喃酮和醚)的分解和碳的表面氧化。
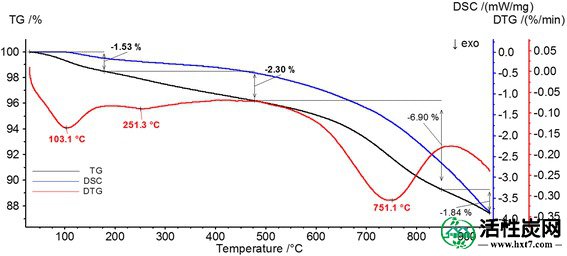
活性炭的热重分析曲线
通过FTIR分析确认在550-950℃的温度范围内发生的过程。在CO 2和CO(波数2000-3000cm -1)的范围特征中的FTIR光谱示于图 3中。他们指出,在600°C以上,CO峰强度增加,这证明了活性炭的醌,羰基,吡喃酮和醚基团的分解[ 34 ]。

活性炭的FTIR光谱。粗体曲线与DTG曲线上的最大值相关联
图 4显示了活性炭分解的主要气态产物的MS曲线:OH(m / z = 17),H 2 O(m / z = 18),CO 2(m / z = 44),SO 2(m / z = 64),和C 6 H 6(m / z = 78)。在低温范围,即30-180°C,有两个峰值,最大值在100°C,H 2 O特征(m / z = 18) - 物理结合水和OH的去除(m / m / m) z = 17) - 去除表面羟基。在100-500°C的温度范围内,CO 2峰值(m / z = 44),最高温度为266°C。C 6 H 6的独特峰(m / z = 78)的温度范围为100-300℃,最高温度为240℃。在300-500℃的温度范围内,存在轻微的峰值,最大值在378℃,并且在高于700℃的高温下SO 2(m / z = 64)进一步强烈增加。对应于m / z = 44的峰与表面羧基的分解有关[ 35 ]。与m / z = 78相关的峰对应于苯环的断裂(例如,通过二硫桥与活性炭表面相关的那些)。通过与m / z = 64有关的峰证明了含硫各种类型表面基团的分解。
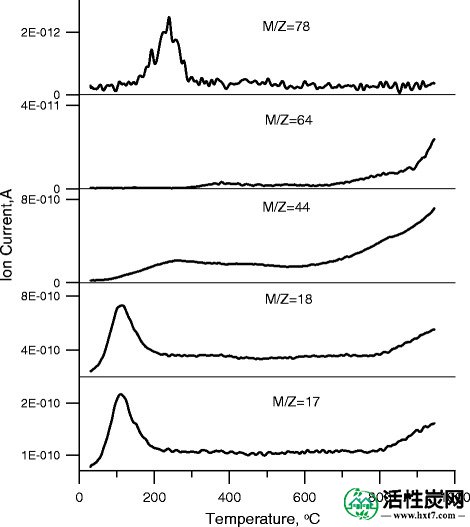
活性炭降解主要产物的MS谱
聚(丙烯酸)在活性炭表面上的吸附等温线示于图2和3中。 5及门6。6。它们在三种溶液pH值(3,6和9)下获得。可以看出,溶液pH值越高,PAA的吸附量越大。这是PAA羧基分解的变化以及HPA表面电荷的符号和密度的变化的结果。
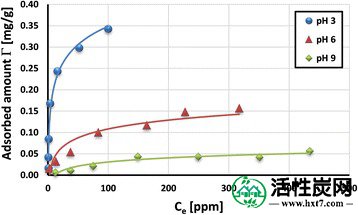
在各种溶液pH值下,PAA 2000 Da在HPA表面上的吸附等温线
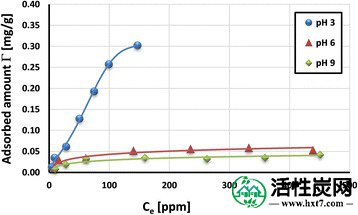
在各种溶液pH值下,HPA表面上PAA 240,000Da的吸附等温线
吸附剂和吸附物之间的静电吸引发生在pH3。在pH3下PAA官能团的解离是最小的,因此,聚合物大分子呈现更卷曲的构象。另一方面,活性炭的表面带正电(HPA的零电荷点为7)。在这样的条件下,聚合物吸附层的结构的特征在于相当大的填充,结果,获得了活性炭表面上最高的PAA吸附水平。
有利静电力的出现不排除吸附剂和吸附物之间形成氢桥,以及疏水相互作用。离解的和未离解的聚(丙烯酸)羧基可以与活性炭表面基团(尤其是含有硫原子的那些)参与形成氢键。另一方面,疏水相互作用可出现在最小解离的聚合物和苯环之间(通过二硫键与表面连接)。
此外,具有较低分子量(即2000 Da)的PAA大分子可以吸附在固体孔内(平均直径为2.26 nm)[ 36 ]。与PAA 240,000 Da链相比,PAA 2000 Da线圈在pH 3下的吸附略高(图 8)。在其他金属氧化物(即氧化锆)的情况下,PAA 2000吸附层的厚度不超过1.2nm,溶液中聚合物线圈的流体动力学半径等于1.5nm [ 37 ]。
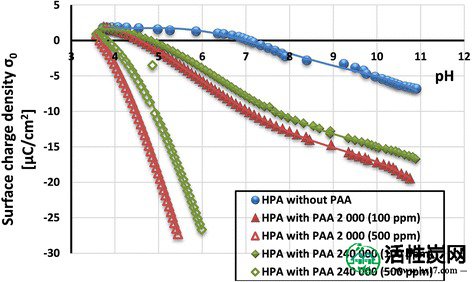
没有和具有聚(丙烯酸)的活性炭的表面电荷密度 - 聚合物分子量和浓度的影响
在pH6和9下观察到显着较低的聚(丙烯酸)吸附量。尽管在pH6下,PAA与活性炭表面之间仍存在吸引人的相互作用,但聚合物链的构象发生显着变化。在这样的条件下,实际上,PAA羧基的总解离发生,并且聚合物链呈现显着延长的构象(与pH 3的那些相比)。吸附的大分子的这种构象消耗HPA表面上的许多活性位点,占据更大的表面积。它们阻挡活性炭表面基团,使其无法被其他吸附链接近。另外,在pH 9下,发生带负电的吸附剂和完全离解的PAA链之间的静电排斥。作为结果, 7)。与具有较高分子量的PAA相比,具有较低分子量的PAA显示出更高的吸附水平。虽然两种聚合物的特征在于延伸构象,但PAA 2000 Da的衬里尺寸远小于PAA 240,000 Da [ 26 ]。因此,具有小尺寸的聚合链具有更大的穿透固体孔(甚至部分)的可能性。
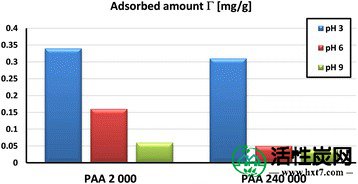
在各种溶液pH值下比较HPA表面上PAA的吸附量
如可在图中可以看出 8,表面电荷密度(σ 0)HPA中的PAA存在显著降低(相比于系统而不PAA)。此外,观察到pH pzc向较低pH值的变化(对于不含PAA的HPA,从pH7到具有PAA 2000Da(500ppm)的HPA的pH3.6)。此外,减少的σ 0活性炭的值越大在PAA的较低分子量的情况下。
所检查体系的这种行为的主要原因是在溶液表面层中吸附的聚合物链中存在带负电荷的羧基。(含有-COOH基团)直接与HPA的表面基团(位于吸附链的列车结构)连接的聚合物链段导致σ的增加0值。在另一方面,位于吸附大分子的尾部和环结构的聚合物链段向σ 0值减少。因此,σ的值0通过实验获得的是这两种效应的总和。获得的结果表明,在所研究的pH范围内,在所检测的系统中,属于位于吸附的PAA链的尾部和环状结构中的链段的解离的羧基的存在的影响必须是显着的(即,3.6-11)。 ,图 8)。
更重要的是,具有较低分子量的PAA更平坦的构象使得它们的链形成更短的尾部和环状结构。由于这个原因,在固 - 液界面处存在大量PAA解离的羧基是造成HPA表面电荷密度更显着降低的原因(与含有PAA 240,000Da的系统相比)。
对于聚(丙烯酸)的两种分子量,聚合物浓度的增加导致HPA表面电荷密度的降低。这是由于含有大量带负电荷的羧基的聚合物吸附层的堆积增加引起的。
对zeta电位测量结果的分析(图 9)得出结论,聚(丙烯酸)在HPA颗粒表面上的吸附导致电动势值的降低。而且,没有聚合物的固体的等电点位于pH3.4。pH值之间的这种大的差异PZC和pH IEP活性炭的值可以是形成中孔壁[根据双电层的重叠的结果38,39 ]。
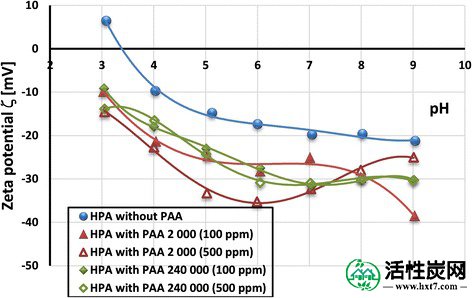
没有和具有聚(丙烯酸)的HPA颗粒的Zeta电位 - 影响聚合物分子量和浓度
根据M'Pandou和Siffert [ 40],阴离子聚合物存在中zeta电位降低的主要原因是在滑动面积区域中聚合物大分子的带电基团(负羧基)的出现。由于存在聚合物吸附层而导致的滑动平面的移动是zeta电位降低的第二个原因。在聚合物大分子在固体表面上呈现更多延伸构象的条件下(即,在更高的PAA浓度下),这种效应是显着的。第三种现象与吸附的大分子对固体表面上活性位点的阻断有关。这种行为是由活性炭表面上的聚合链的扁平构象引起的。从而,
通过超临界萃取啤酒花(HPA)后残留物的物理活化获得的活性炭上形成的聚(丙烯酸)吸附层的纳米结构被表征。已经证明,具有较低分子量(2000Da)的PAA在pH3下在固 - 液界面处表现出最高的吸附。在这样的条件下,PAA大分子假定最大的卷曲结构(聚合物羧基的轻微离解)。带正电荷的固体表面和聚合物线圈之间的静电引力导致形成由致密堆积的大分子组成的吸附层。此外,在pH 3 PAA下,具有较低分子量的大分子可以穿透平均直径为2.26nm的固体孔。除了静电力,
HPA表面上的聚(丙烯酸)吸附导致固体颗粒的表面电荷密度和ζ电位降低(与不含聚合物的系统相比)。这种行为的主要原因是在溶液的表面层中存在带负电荷的聚合物链段(属于吸附的大分子)(导致固体表面电荷密度降低)和滑动平面区域(导致还原) zeta电位)。